अधिशोषक द्वारा अधिशोषित गैस की मात्रा में स्थिर ताप पर दाब के साथ परिवर्तन एक वक्र के माध्यम से व्यक्त किया जा सकता है जिसे हम अधिशोषण समतापी (Adsorption Isotherm ) कहते हैं।
फ्रॉयंडलिक अधिशोषण समतापी (Freundlich Adsorption Isotherm ) फ्रॉयंडलिक ने 1909 में ठोस अधिशोषक के इकाई द्रव्यमान द्वारा एक निश्चित ताप पर अधिशोषित गैस की मात्रा एवं दाब के मध्य एक सम्बन्ध स्थापित किया। इसके अनुसार दाब बढ़ाने पर अधिशोषण की मात्रा बढ़ जाती है। जब अर्थात् अधिशोषण की मात्रा अधिकतम होती है तब वह दाब साम्यावस्थिक दाब कहलाता है। साम्यावस्थिक दाब पर अधिशोषण अधिकतम होता है तथा और अधिक दाब बढ़ाने पर भी अधिशोषण की मात्रा नहीं बढ़ती है। यहाँ अधिशोषण का मान नियत हो जाता है।
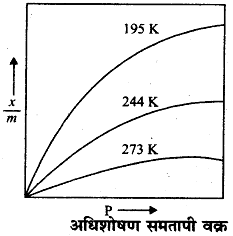
कम दाब पर (At low pressure) कम दाब पर वक्र लगभग एक सीधी रेखा होती है अर्थात्
\(\frac{x}{m} ∝ p^1\)
\(\frac{x}{m} = kp^1\)
अधिक दाब पर (At high pressure) उच्च दाब पर x/m का मान लगभग स्थिर हो जाता है। अर्थात्
\(\frac{x}{m} ∝ p^0\)
था
\(\frac{x}{m} = kp^0\)
मध्यम दाब पर (At intermediate pressure) मध्यम दाब पर x/ms का मान दाब की घात पर निर्भर करता है।
\(\frac{x}{m} ∝ p^{1/n}\)
यहाँ x > 1
\(\frac{x}{m} = kp^{1/n}\)
उपर्युक्त समीकरण का log लेने पर,
log \(\frac{x}{m}\) = log k + \(\frac{1}{n}\) log p
उपर्युक्त समीकरण फ्रॉयन्डलिक समतापी वन समीकरण कहलाता फ्रॉयन्डलिक समतापी वक़ की वैधता, आलेख में log: कोy. अक्ष (कोटि) एवं logp को x-अक्ष (भुज) पर लेकर प्रमाणित की जा सकती है। यदि यह एक सीधी रेखा आती है तो फ्रॉयन्डलिक समतापी वक्र प्रमाणित है अन्यथा नहीं।
सीधी रेखा का ढाल - का मान देता है। -अक्ष पर अन्त:खण्ड - logk का मान देता है।

फ्रॉयडलिक समतापी वक्र यह भी जानेंप्रायोगिक समतापी सदैव उच्च दाब पर संतृप्तता की ओर अभिगमन करते प्रतीत होते हैं। इसे फ्रॉयन्डलिक समतापी वक्र से नहीं समझाया जा सकता, अत: यह उच्च दाब पर असफल हो जाता है।